Autora:
Lewis Jackson
Data De La Creació:
5 Ser Possible 2021
Data D’Actualització:
1 Juliol 2024

Content
Mol és la unitat de mesura estàndard en química, que s’utilitza per mirar els diferents elements d’un compost. Normalment, la massa composta es calcula en grams (g) i s’ha de convertir en unitats molars. La transició és força senzilla, però, encara hi ha alguns passos importants que hem de seguir. Mitjançant el mètode següent, podeu convertir fàcilment grams en lunars.
Passos
Part 1 de 2: Calculeu la massa molecular
Prepareu els subministraments necessaris per resoldre el problema matemàtic. Quan tingueu totes les eines disponibles, serà més fàcil resoldre el problema. El que necessiteu és:
- Llapis i paper. Les matemàtiques es fan més fàcils quan ho escriviu tot en paper. Cal presentar tots els passos per aconseguir la màxima puntuació.
- Taula periòdica d'elements químics: s'utilitza per determinar els àtoms de massa dels elements.
- Calculadora de butxaca: s’utilitza per calcular nombres complicats.

Determineu quins elements del compost heu de convertir a unitats molars. El primer pas per calcular la massa molecular és determinar els elements que formen el compost. Això és fàcil perquè l'abreviatura d'elements només té un o dos caràcters.- Si una substància s’abrevia amb dues lletres, la primera lletra es posarà en majúscula i la segona lletra en minúscula. Exemple: Mg és l'abreviatura de l'element magnesi.
- Compostos de NaHCO3 consta de quatre elements: sodi (Na), hidrogen (H), carboni (C) i oxigen (O).
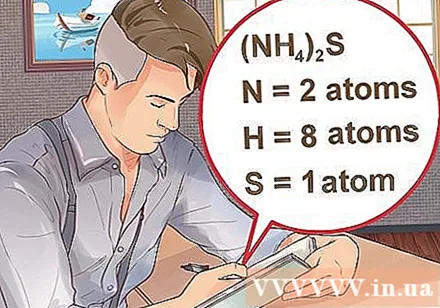
Determineu el nombre d’àtoms per a cada element del compost. Cal calcular el nombre atòmic de cada substància d’un compost per calcular la molècula de massa d’aquest compost. El nombre petit situat al costat de l'abreviatura de l'element representa el nombre atòmic de l'element.- Exemple: compost H2O té dos àtoms d’hidrogen i un d’oxigen.
- Si un compost s’escriu entre parèntesis, acompanyat d’un índex petit, vol dir que cada ingredient entre parèntesis multiplica l’índex. Exemple: compost (NH4)2S consta de dos àtoms N, vuit àtoms H i un àtom S.

Anoteu el paper atòmic cúbic de cada element. L’ús de la taula periòdica és la forma més senzilla de trobar l’àtom cúbic d’un element. Després de localitzar l'element a la taula periòdica, veureu la massa atòmica just a sota de la icona de l'element.- Per exemple, l'àtom cúbic d'oxigen és de 15,99.
Calculeu la massa molecular. La molècula de massa d’una substància és igual al nombre d’àtoms de cada element multiplicat per l’àtom de massa d’aquest element. Aquesta quantitat és essencial en la conversió de gram a molar.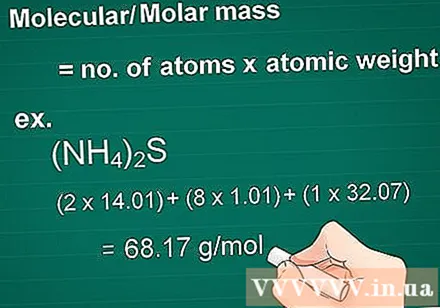
- En primer lloc, multiplica el nombre atòmic de cada element del compost pel seu àtom de massa.
- A continuació, afegiu les masses dels elements del compost junts.
- Exemple: massa molecular d’un compost (NH4)2S = (2 x 14,01) + (8 x 1,01) + (1 x 32,07) = 68,17 g / mol.
- La massa molecular també es coneix com a massa molar.
Part 2 de 2: converteix els grams en mol
Configureu la fórmula de conversió. Per trobar el nombre de mols del compost, divideix el nombre de grams del compost per la massa molar d’aquest compost.
- Fórmula: nombre de mols = massa (grams) / massa molar del compost (gram / mol)
Introduïu els números a la fórmula. Després de configurar la fórmula adequada, el pas següent és substituir els nombres que heu calculat per la fórmula. Si voleu assegurar-vos que les dades estiguin en la posició correcta, podeu comprovar-les suprimint la unitat. Si després de la simplicitat la unitat restant són mols, estareu configurat correctament.
Resol l’equació. Amb una calculadora, divideix la massa per la molècula cúbica de la substància o compost. El quocient serà el nombre de mols de la substància o compost que esteu cercant.
- Per exemple, el problema és de 2 g d’aigua (H2O) i demanar-li que el converteixi en unitats molars. Tenim la massa molar d’H2O és 18 g / mol. Dividiu 2 per 18, de manera que tingueu 0.1111 mol H2O.
Consells
- No oblideu incloure l’element o el nom compost amb les respostes.
- Si se us demana que presenteu un exercici o un qüestionari, assegureu-vos de mostrar les vostres respostes clarament donant voltes o dibuixant un quadre al voltant de les respostes.
Què necessites
- Taula periòdica química
- Llapis
- Paper
- Ordinador
- Problemes de química