Autora:
Louise Ward
Data De La Creació:
11 Febrer 2021
Data D’Actualització:
1 Juliol 2024

Content
La mida d’un àtom és tan petita que és difícil mesurar amb precisió el nombre atòmic d’un compost químic. Per poder mesurar amb precisió una quantitat de substàncies, els científics utilitzen una unitat de mol per representar un nombre especificat d'àtoms. Un mol de substància es defineix com l’equivalent al nombre d’àtoms de carboni continguts en 12 grams de l’isòtop de 12 carboni, que és d’uns 6.022 x 10 àtoms. Aquest valor s’anomena número Avogadro o constant d’Avogadro. Això també es coneix com el nombre d’àtoms en 1 mol de qualsevol element, i 1 mol de la massa d’una substància s’anomena massa molar d’aquesta substància.
Passos
Mètode 1 de 2: Calculeu la massa molar d’un element
Definició de massa molar. La massa molar d’una substància és la massa (en grams) d’un mol d’aquesta substància. Per calcular la massa molar d’un element, multiplica la seva massa atòmica pel factor de conversió gram per mol (g / mol).
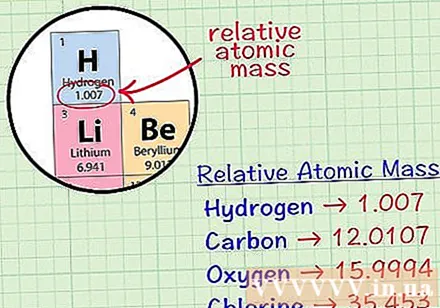
Trobeu l’àtom cúbic mitjà d’un element. L’àtom de massa mitjana d’un element és la massa mitjana, en unitats atòmiques, d’una mostra que inclou tots els isòtops d’aquest element. Aquesta informació es dóna sovint a la taula periòdica d’elements. En localitzar un element, podeu trobar un àtom cúbic mitjà escrit just a sota del símbol químic de l’element. Aquest valor no és un nombre enter, sinó un nombre amb decimals.- Per exemple, amb l'hidrogen, l'àtom de massa mitjà és d'1,007; L’àtom cúbic mitjà de carboni és de 12.0107; L’àtom de massa mitjana d’oxigen és de 15.9994; el clor té una massa atòmica mitjana de 35.453.

Multiplicar l'àtom de massa mitja per la constant de massa molar. La unitat de lliscament molar es defineix com 0,001 quilograms per mol, o 1 gram per mol. El producte de l’àtom de massa mitjana i la constant de massa molar converteix la unitat de massa atòmica en grams per mol, de manera que la massa molar de l’hidrogen serà de 1,007 grams per mol, per al carboni és de 12 , 0107 grams per mol, d’oxigen són 15.9995 grams per mol, i el de clor és de 35.453 grams per mol.- Alguns elements existeixen a la natura com a molècules que consisteixen en dos o més dels mateixos àtoms. És a dir, si voleu calcular la massa molar dels compostos formats per més d’un àtom, com ara l’hidrogen gasós, l’oxigen gasós o el clor gasós, heu de determinar la massa atòmica mitjana del compost i multiplicar aquest valor. amb la constant de massa molar, "" després "multiplica el producte que acabes de trobar per 2.
- Amb H2: 1.007 x 2 = 2.014 grams per mol; per a O2: 15.9994 x 2 = 31.9988 grams per mol; i Cl2: 35.453 x 2 = 70.096 grams per mol.
Mètode 2 de 2: Calculeu la massa molar del compost

Determineu la fórmula estructural del compost. La fórmula estructural d’una substància dóna el nombre atòmic de cada element que compon aquest compost. (Aquesta informació està disponible a tots els llibres de consulta). Per exemple, la fórmula química de l'àcid clorhídric és HCl; de glucosa és C6H12O6. Amb aquesta fórmula estructural, podem determinar el nombre de cada tipus d’àtom que constitueix el compost considerat.- On l’HCl té un àtom d’hidrogen i un de clor.
- Molècula C de sucre de glucosa6H12O6 té 6 àtoms de carboni, 12 àtoms d’hidrogen i 6 àtoms d’oxigen.
Determineu l’àtom de massa mitjà de cada element constituent. Utilitzeu la taula periòdica per trobar l'àtom de massa mitjana de cada element present en el compost. L’àtom de massa mitjana s’escriu normalment sota el símbol químic de l’element a la taula periòdica. De manera similar al càlcul de la massa molar d’un element, multiplica l’àtom de massa mitjà per 1 gram / mol.
- L’àtom de massa mitjà dels elements que formen àcid clorhídric és el següent: hidrogen 1.007 g / mol i clor 35.453 g / mol.
- L’àtom de massa mitjà dels elements que formen la molècula de glucosa és: carboni, 12.017 g / mol; hidrogen, 1.007 g / mol; i oxigen, 15,9995 g / mol.
Calculeu la massa molar de cada element component. Multiplicant l'àtom de massa d'un element pel nombre d'àtoms que aporta en un compost es dóna la massa mitjana de l'element del compost.
- En el cas de l’àcid clorhídric, HCl, la massa molar de l’element hidrogen és de 1.007 g / mol, i la del clor és de 35.453 g / mol.
- En el cas de la glucosa, C6H12O6, la massa molar de cada element és la següent: carboni, 12.0107 x 6 = 72.0642 g / mol; hidrogen, 1.007 x 12 = 12.084 g / mol; oxigen, 15.9995 x 6 = 95.9964 g / mol.
Massa molar total dels elements constitutius. La massa molar total dels elements de compostatge és la massa molar del compost.En el pas anterior vam calcular la massa molar de cada element present en el compost, en aquest pas només hem de sumar tots aquests valors junts.
- La massa molar d’àcid clorhídric és de 1.007 + 35.453 = 36.460 g / mol. 36,46 grams és la massa de 1 mol d’àcid clorhídric.
- La massa molar de glucosa és de 72.0642 + 12.084 + 95.9964 = 180.146 g / mol. Per tant, cada mol de glucosa té una massa de 180,14 grams.
Consells
- Encara que en la majoria dels casos, l'àtom de massa mitjana es registra fins a la part més propera a 1000 (4 decimals), en els laboratoris, la massa molar sovint es redueix a 2 decimals, de vegades encara menys, per a molècules grans. Per tant, en el cas de laboratori, la massa molar d’àcid clorhídric es pot escriure com a 36,46 g per mol, per a la glucosa 180,14 g per mol.
Què necessites
- Llibre de consulta química o taula periòdica d’elements
- Ordinador